Нарушение репродуктивной функции женщины может явиться следствием повышения уровня мужских половых гормонов в крови (андрогенов), избыток которых в организме женщины связан с нарушением работы яичников или надпочечников, которые ответственны за выработку этих гормонов.
Остановимся коротко на основных терминах, которые используются при данной патологии.
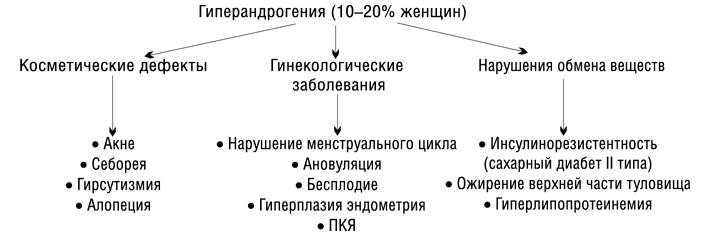
Гиперандрогенемия — повышенная концентрация андрогенов в сыворотке крови, которая проявляется, в большинстве случаев, андрогенизацией (гирсутизм, алопеция, угревая сыпь). Так, частота гирсутизма при гиперандрогении составляет около 80%.
Распространенность гиперандрогении составляет 10%.
Андрогенизация — проявление симптомов, типичных для высокого уровня андрогенов (гирсутизм, алопеция, угревая сыпь и вирилизация).
Гирсутизм – заболевание, при котором у женщин рост и распределение терминальных волос происходит по мужскому типу.
Алопеция — видимое на глаз разрежение волос на голове с появлением проплешин. Наиболее частая форма – андрогенетическая алопеция (распространенность составляет 30-40%), чаще наблюдается у женщин в перименопаузе (за счёт физиологического повышения уровня андрогенов).
Угри (акне) — заболевание сальных желез волосяных фолликулов. Распространенность обыкновенных угрей среди подростков составляет 35-90% . У юношей акне наблюдается чаще, чем у девушек, а в более позднем возрасте соотношение мужчин и женщин с угревой сыпью обратное –у женщин больше, чем мужчин. С возрастом частота акне уменьшается: у женщин 20-29 лет она составляет 51%, старше 50 лет – 15%.
Вирилизация — появление у женщин мужских черт телосложения и мужских вторичных половых признаков (низкий тембр голоса, увеличение гортани, мужские пропорции тела, увеличение клитора гирсутизм).
Гиперадрогения – андрогенизация без повышения уровня андрогенов в крови (гиперандрогенемии).
Гипертрихоз — рост волос на участках тела, не характерный для данного пола, и появление терминальных волос на участках, где в норме растут пушковые волосы.
Симптомы андрогенизации – одна из причин обращения к гинекологу за консультацией. Данные симптомы могут встречаться при следующих заболеваниях:
- синдром поликистозных яичников (СПКЯ) (см. раздел СПКЯ);
- врожденный адреногенитальный синдром (АГС);
- андрогенпродуцирующия опухоль яичника (редкая опухоль – 1% от всех опухолей яичника);
- синдром Кушинга.
При симптомах андрогенизации необходимо сдать следующие анализы на гормоны: общий тестостерон, ДГЭАС, 17 – ОНР, эстрадиол, ЛГ, ФСГ, ТТГ, пролактин, кортизол. При необходимости на втором этапе проводят пробы с дексаметазоном, пробу с гормоном АКТГ.
Внизу остановимся коротко на каждом из этих заболеваний.
Врожденный АГС — адреногенитальный синдром, или врожденная гиперплазия надпочечников.
Врожденный АГС, или врожденная гиперплазия надпочечников — общее название нескольких наследуемых дефектов ферментов, участвующих в биосинтезе кортизола в надпочечниках. Наиболее частым из них является недостаточность фермента 21 – гидроксилазы (в 95% случаев). В зависимости от степени недостаточности дефектного фермента различают тяжелую (классическую) и легкую (неклассическую, или позднею) формы АГС.
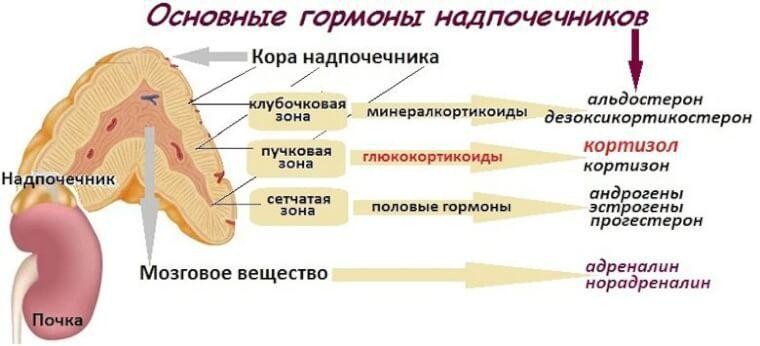
Биосинтез стероидных гормонов происходит в коре надпочечников:
- минералокортикоиды синтезируются в клубочковой зоне,
- глюкокортикоиды – в пучковой,
- половые гормоны — в сетчатой зоне.
Главными источниками половых гормонов являются половые железы. Продукции половых гормонов корой надпочечников придают функ-циональное значение только в необычных условиях, когда на путях биосинтеза в надпочечных железах появляются дефекты ферментов.
При АГС, в зависимости от дефектного фермента, отмечаются различные типы нарушения биосинтеза стероидных гормонов.
Внизу представлена схема образования гормонов с участием различных ферментов.
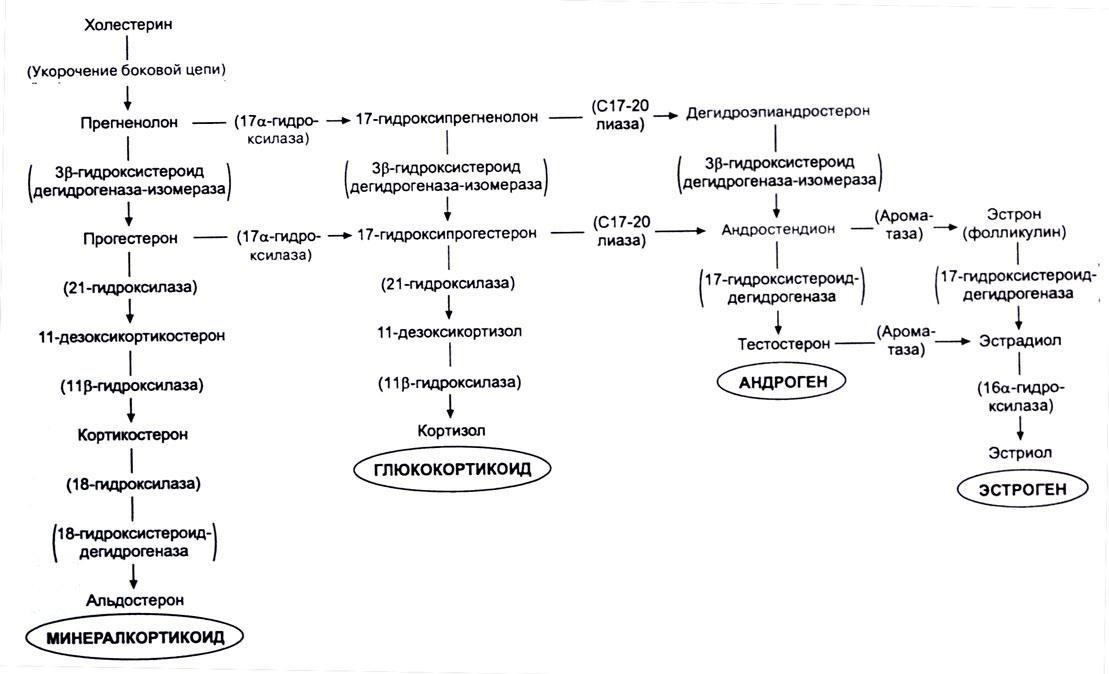
Например, при недостаточности фермента 21 – гидроксилазы, нарушается превращение 17 – ОНР (17 – гидроксипрогестерона) в 11 – дезоксикортизол, в результате снижается синтез кортизола в надпочечниках, в ответ повышается секреция АКТГ гипофизом. АКТГ стимулирует кору надпочечников, в результате чего, из 17 – ОНР синтезирируются андрогены, уровень которых повышается.
Лабораторная диагностика непосредственно гиперандрогенемии основывается на определении общего тестостерона, ДГЭАС и 17 – ОНР.
При определении концентрации андрогенов в сыворотке крови, говорить о принадлежности этих гормонов к тому или иному секретирующему органу — надпочечникам или половым железам, можно лишь условно.
Так, 50% ДГЭАС образуется в коре надпочечников, 25% в яичниках и 25% в периферических тканях. 50% тестостерона синтезируется в периферических тканях, остальное количество – в яичниках 25% и коре надпочечников 25%.
Классическая форма АГС обычно диагностируется в детстве, и поэтому рассматривать ее мы не будем.
Неклассическая (поздняя, или легкая) форма АГС проявляется только клиническими признаками избыточной выработки андрогенов, усиливающимися с возрастом. Клинические признаки избытка андрогенов у подростков и взрослых: угри – 30% случаев, гирсутизм – 60-90% случаев, алопеция – меньше 10% случае, нарушение менструального цикла, например олигоменорея – 55% случаев или аменорея – 5% случаев, бесплодие – 15% случаев.
Следует обратить внимание, что для уменьшения проявлений андрогенизации, глюкокортикоиды не являются препаратами выбора. При бесплодии, для стимуляции овуляции кортикостероиды применяются только в случае АГС с поздним началом. Обычно назначают гидрокортизон в дозе 10-20 мг 2 раза в сутки или дексаметазон в дозе 0,25- 0,5 мг 1 раз в сутки.
Андрогенпродуцирующая опухоль.
Андрогенпродуцирующие опухоли проявляются быстрым проявлением симптомов андрогенизации. В том случае, если уровень андрогенов невысокий, но гирсутизм или вирилизация прогрессируют, то в первую очередь, следует исключить андрогенпродуцирующую опухоль. Опухоли поражают в основном яичники и реже выявляются в надпочечниках.
Диагностика: УЗИ яичников, МРТ надпочечников.
Синдром Кушинга
Синдром гиперкортицизма или синдром Иценко — Кушинга объединяет группу заболеваний, при которых происходит длительное хроническое воздействие на организм избыточного количества гормонов коры надпочечников, независимо от причины, которая вызвала повышение количества этих гормонов в крови. В основе патологических изменений со стороны большинства органов и систем, при синдроме Кушинга, в первую очередь, лежит гиперпродукция кортизола.
Синдром Кушинга также может возникать при первичном поражении коры надпочечников (при доброкачественных или злокачественных опухолях коры надпочечников, при гиперплазии коры надпочечников).
Гормонально-активная опухоль коры надпочечника называется кортикостеромой. Она продуцирует в кровь избыточное количество глюкокортикоидов. При этом, из-за избыточного количества глюкокортикоидов, по механизму обратной связи, снижается количество адренокортикотропного гормона гипофиза, а оставшаяся ткань надпочечников подвергается атрофическим изменениям.
Синдром гиперкортицизма может возникнуть при лечении различных заболеваний гормонами коры надпочечников — глюкокортикоидами, в случае, если происходит передозировка этих препаратов. Это является частым вариантом, с которым сталкиваются врачи большинства специальностей. Болеют в основном лица в возрасте 20—40 лет.
Гиперсекреция кортизола, также довольно часто может наблюдаться при ожирении, хронической алкогольной интоксикации, беременности и некоторых психических и неврологических заболеваниях — такое состояние называется «Псевдо-Кушинга синдром» или «функциональный гиперкортицизм», который не вызван опухолями, но клиническая картина наблюдается как и при истинном синдроме Иценко — Кушинга.
Помимо синдрома, отдельно выделяют болезнь Иценко — Кушинга — это нейроэндокринное заболевание, характеризующееся повышенной продукцией гормонов коры надпочечников, которая обусловлена избыточной секрецией АКТГ клетками гиперплазированной или опухолевой ткани гипофиза (в 90% это микроаденома).
Диагностика
При подозрении на синдром Иценко — Кушинга (повышение уровня общего кортизола в сыворотке крови) выполняются различные пробы с дексаметазоном и выполняется двух- или трехкратное определение свободного кортизола в суточной моче.
Лечение заболевания зависит от результатов обследования, т. е. от того, в какой именно области выявлен патологический процесс, приведший к возникновению гиперкортицизма.
На сегодняшний день единственным, действительно эффективным методом лечения болезни Иценко–Кушинга, возникшей в результате аденомы гипофиза, является хирургический, при котором проводится селективная транссфеноидальная аденомэктомия. Эта нейрохирургическая операция показана при выявлении аденомы гипофиза, локализация которой чётко была установлена при обследовании. У подавляющего числа больных, эта операция дает положительные результаты. Достаточно быстро происходит восстановление нормального функционирования гипоталамо-гипофизарной системы, в 70–80 % случаев наступает стойкая ремиссия заболевания. Однако у 10–20 % пациентов может возникнуть рецидив.
Хирургическое лечение болезни Иценко–Кушинга обычно сочетается с лучевой терапией, а также методом деструкции гиперплазированных надпочечников (т. к. масса желез увеличивается в результате длительного гормонального сбоя).
При наличии противопоказаний к хирургическому лечению аденомы гипофиза (тяжелое состояние пациентки, наличие тяжелых сопутствующих заболеваний и др.), проводится медикаментозное лечение.
Применяются препараты, которые подавляют секрецию адренокортикотропного гормона (АКТГ), повышение уровня которого и приводит к гиперкортицизму. На фоне такого лечения, при необходимости, обязательно проводится и симптоматическая терапия гипотензивными, сахароснижающими препаратами, антидепрессантами, лечение и профилактика остеопороза и др.
Если причиной возникновения гиперкортицизма стали опухоли надпочечников или других органов, то необходимо их удаление. При удалении пораженной надпочечниковой железы, с целью профилактики гипокортицизма в дальнейшем, больным будет необходима длительная заместительная гормональная терапия под постоянным контролем врача.
Адреналэктомия (удаление одного или двух надпочечников) в последнее время используется редко, только в случае невозможности лечения гиперкортицизма другими способами. Эта манипуляция приводит к хронической надпочечниковой недостаточности, требующей пожизненной заместительной гормональной терапии.
Все пациенты, которым было проведено или проводится лечение этого заболевания, нуждаются в постоянном наблюдении эндокринолога, а при необходимости, и других специалистов.